Ząbkowanie, histamina i bariera krew-mózg: Dlaczego ten okres jest kluczowy dla bezpieczeństwa dziecka?
Autor opracowania: Piotr Jawornik
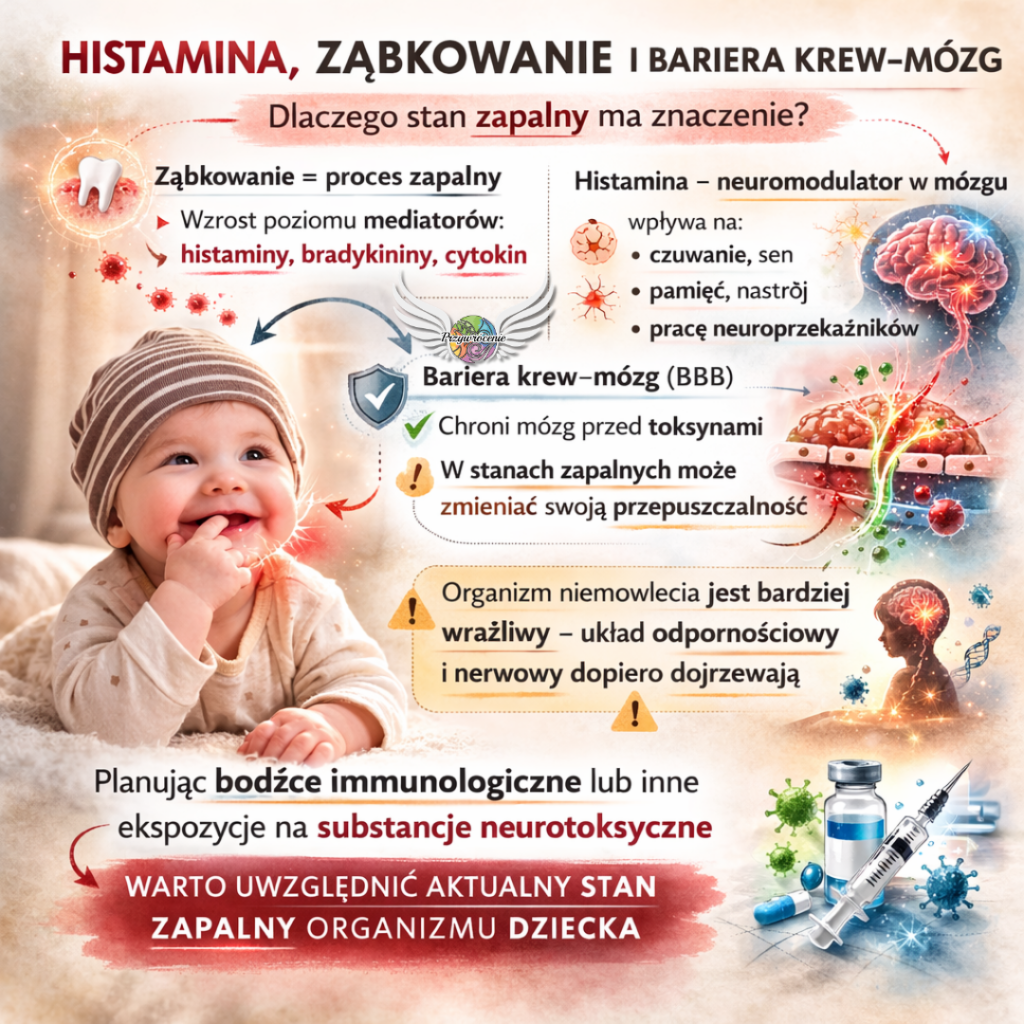
W rozwoju dziecka istnieje niewiele procesów tak powszechnych, a jednocześnie tak obciążających organizm, jak ząbkowanie. Choć często traktowane jedynie jako dyskomfort, z punktu widzenia neurobiologii i immunologii jest to złożony stan zapalny, który ma bezpośredni wpływ na szczelność bariery krew-mózg oraz gospodarkę neurochemiczną organizmu.
1. Ząbkowanie
Ząbkowanie wiąże się z ogromnym obciążeniem mechanicznym. Wzrost zębów powoduje rozrywanie tkanek i komórek, co skutkuje uwolnieniem zawartości wewnątrzkomórkowej do przestrzeni zewnątrzkomórkowej. To z kolei aktywuje komórki układu odpornościowego do uwalniania tzw. „czynników prozapalnych”.
W procesie tym biorą udział kluczowe mediatory stanu zapalnego:
- Bradykinina: powoduje rozszerzenie naczyń krwionośnych.
- Histamina: kluczowa cząsteczka sygnałowa, która odpowiada za zaczerwienienie, ciepło i obrzęk dziąseł.
Warto pamiętać, że stan zapalny może przebiegać „po cichu” – nie zawsze wszystkie pięć klasycznych objawów (ból, guz, kolor, ciepło, utrata funkcji) jest widocznych gołym okiem, jednak procesy chemiczne wewnątrz organizmu zachodzą z pełną siłą.
2. Rola histaminy w układzie nerwowym
Histamina nie jest tylko mediatorem alergii. To potężny regulator funkcji mózgu. Jedynym źródłem neuronów histaminergicznych jest tylne podwzgórze (jądro tuberomamillare – TM), które unerwia cały centralny układ nerwowy.
System histaminergiczny odpowiada za:
- Stan czuwania i metabolizm: Neurony te działają wyłącznie podczas czuwania.
- Procesy uczenia się i pamięć: Poprzez receptory H3 histamina wspiera układy limbiczne.
- Modulację innych neuroprzekaźników: Aktywacja receptorów H3 może zmniejszać uwalnianie acetylocholiny, dopaminy, noradrenaliny i serotoniny.
3. Bariera krew-mózg a zagrożenie neurotoksynami
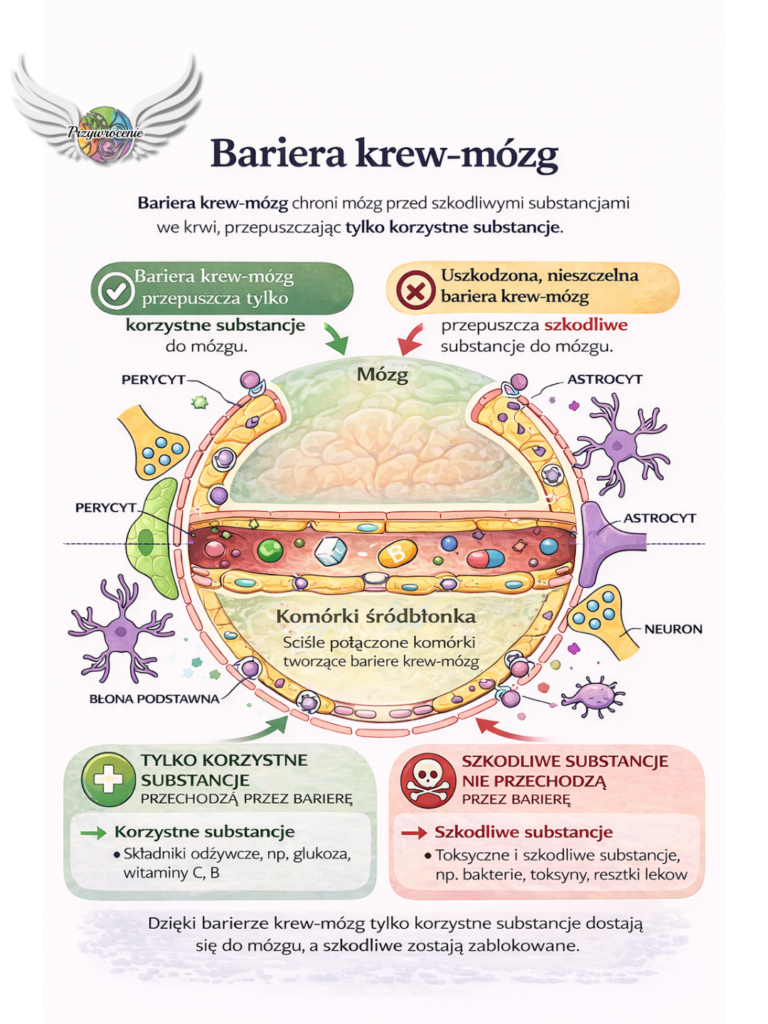
Kluczowym zagadnieniem podniesionym w materiałach źródłowych jest wpływ histaminy na barierę krew-mózg (BBB). W normalnych warunkach bariera ta jest niemal nieprzepuszczalna dla dużych cząsteczek i toksyn, chroniąc mózg przed szkodliwymi czynnikami krążącymi we krwi.
Jednakże uwalnianie dużej ilości histaminy podczas stanu zapalnego (np. przy ząbkowaniu) powoduje zmiany naczyniowe. Histamina zwiększa przepuszczalność bariery krew-mózg, co w literaturze medycznej określa się jako jej „rozszczelnienie”.
4. Adiuwanty i szczepienia w okresie ząbkowania
Adiuwanty, takie jak związki glinu, są dodawane do szczepionek. W momencie, gdy organizm dziecka znajduje się w fazie aktywnego ząbkowania:
- Otwarta brama: Podwyższony poziom histaminy osłabia barierę krew-mózg.
- Dostęp do OUN: Substancje, które normalnie zostałyby zatrzymane przez barierę (adiuwanty, potencjalne neurotoksyny), mogą uzyskać bezpośredni dostęp do tkanki mózgowej.
- Ryzyko powikłań: Obecność obcych substancji w mózgu może prowadzić do aktywacji mikrogleju, neurostanu zapalnego, a w skrajnych przypadkach do uszkodzenia neuronów.
Podsumowanie
Zrozumienie mechanizmu działania układu histaminergicznego rzuca nowe światło na bezpieczeństwo procedur medycznych w okresach osłabienia organizmu. Ząbkowanie, jako proces generujący wysoką podaż histaminy, stwarza specyficzne warunki biologiczne, w których bariera krew-mózg nie pełni swojej funkcji ochronnej w sposób optymalny. Wybór odpowiedniego momentu na stymulację układu odpornościowego powinien zatem uwzględniać aktualny stan zapalny organizmu dziecka.
Źródła:


[01]PubMed Health. – Inflammation | PMHT: 0022625
[02]PubMed Health. – Immune system | PMHT: 0025680
[03]PubMed Health. – Sense of smell | PMHT: 0025081
[04]PubMed Health. – Cells of the human body | PMHT: 0022040
[05]PubMed Health. – Tissues of the human body | PMHT: 0022306
[06]PubMed Health. – Hormones | PMHT: 0022075
[07]PubMed Health. – Histamine | PMHT: 0025446
[08]PubMed Health. – Blood vessels | PMHT: 0022370
[09]Haas et al. – The role of histamine and the tuberomamillary nucleus in the nervous system | doi: 10.1038/nrn1034
[09a]Scott T. Brady. – Basic Neurochemistry – Principles of Molecular, Cellular and Medical Neurobiology – Eighth Edition
| ISBN: 978-0-12-374947-5
[10] Panula, P., Yang, H. Y. & Costa, E. – Histamine-containing neurons in the rat hypothalamus. Proc. Natl Acad. Sci. USA 81, 2572–2576
(1984). The first direct demonstration of the histaminergic system in the brain; see also reference 11
[11] Watanabe, T et al. – Distribution of the histaminergic neuron system in the central nervous system of rats: a fluorescent
immunohistochemical analysis with histidine decarboxylase as a marker. Brain Res. 295, 13–25 (1984). The first direct demonstration
of the histaminergic system in the brain; see also reference 10. The research group oh Hiroshi Watanabe represented a major focus of histimanine research
[12]Haas et al. – Histamine in the nervous system | doi: 10.1152/physrev.00043.2007
[13]Bouthenet, M. L., Ruat, M., Sales, N., Garbarg, M. & Schwartz, J. C. – A detailed mapping of histamine histamine H receptors in guinea-pig central nervous system established by audiography with iodolpyramine | doi: 10.1016/0306-
4522(88)90167-4
TheJ.C. Schwartz and his group have made some of the most important contributions in the fields of biochemistry and pharmacology of histamine in the brain. They
detected and characterized the H2-autoreactor
[14]Haas et al. – Histamine in the nervous system | doi: 10.1152/physrev.00043.2007
[15]Sakai et al. – Sleep-Waking Discharge of Ventral Tuberomammillary Neurons in Wild-Type and Histidine
Decarboxylase Knock-Out Mice | doi: 10.3389/fnbeh.2010.00053
[16]Vincent S.R et al. – Hypothalamic gamma-aminobutyric acid neurons project to the neocortex | doi:
10.1126/science.6857253
[17]Takeda N. et al. – Immunohistochemical evidence for the coexistence of histidine decarboxylase-like and glutamate
decarboxylase-like immunoreactivities in nerve cells of the magnocellular nucleus of the posterior hypothalamus of
rats | pmid: 6594708
[18]Ericson et al. – GABA-like immunoreactivity in the tuberomammillary nucleus: An electron microscopic study in the
rat | doi: 10.1002/cne.903050309
[19]Jack R.Cooper et al. – The Biochemical Basis of Neuropharmacology | ISBN-10: 0-19-514007-9
[20]Helmut Haas & Pertti Panula – The role of histamine and the tuberomamillary nucleus in the nervous system |
doi: 10.1038/nrn1034
[21]Parmentier et al. – Anatomical, Physiological, and Pharmacological Characteristics of Histidine Decarboxylase
Knock-Out Mice: Evidence for the Role of Brain Histamine in Behavioral and Sleep–Wake Control | PMID: 12196593
[22]Cangioli et al. – Activation of histaminergic H3 receptors in the rat basolateral amygdala improves expression of
fear memory and enhances acetylcholine release | doi: 10.1046/j.1460-9568.2002.02092.x
[23]Baldi et al. – The H3
receptor protean agonist proxyfan enhances the expression of fear memory in the rat | doi:
10.1016/j.neuropharm.2004.09.009
[24]Divya Vohora –The Third Histamine Receptor: Selective Ligands as Potential Therapeutic Agents in CNS Disorders |
ISBN-10: 1-4200-5392-2
[25]Rubio et al. – Improvement of spatial memory by (R)-alpha-methylhistamine, a histamine H(3)-receptor agonist, on
the Morris water-maze in rat | doi: 10.1016/S0166-4328(01)00328-X